聯絡我們
CONTACT
本平台目的為推廣台灣臨床試驗,提供廠商、研究者及一般民眾臨床試驗之相關訊息。 若您需要刊登受試者招募廣告、臨床試驗相關活動或臨床試驗受托機構訊息,歡迎留下您的資料與聯絡方式,我們會儘速跟您連繫。
若有臨床試驗設計規劃上的諮詢需求,歡迎至財團法人醫藥品查驗中心(CDE)網站的諮詢輔導專區,填寫資料後送出,會有專人與您連繫。
Q31
CTD模組一 1.15 國內BA/BE 試驗現況,須要陳述哪些內容?
Q32
CTD 3.1模組三目錄/Table of Contents of Module 3,現已編列5個階層,如有需要,可否再延伸至第六階層?
Q33
3.2.S.3.2不純物是否須要提供結構鑑定及/或安全性資料?
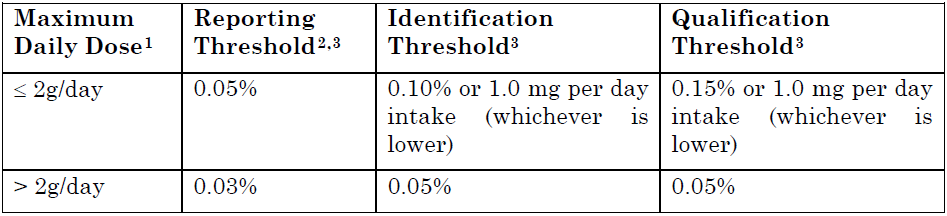
 2.不純物種類、結構分析以及批次分析結果(包括臨床、非臨床及安定性試驗批次等)可於此章節加以詳細描述,並說明這些不純物是否被列入規格中。
2.不純物種類、結構分析以及批次分析結果(包括臨床、非臨床及安定性試驗批次等)可於此章節加以詳細描述,並說明這些不純物是否被列入規格中。
Q34
3.2.S.4.5規格合理性之依據(名稱、製造廠)/Justification of Specification (name, manufacturer)需要陳述哪些內容?
Q35
3.2.P.2.1.1,一般化學藥品需要陳述哪些內容?
Q36
有關探討具特殊功能之賦形劑(functional excipients)於架儲期間所發揮效能之相關資料,應於何章節段落呈現?
Q37
包裝系統中,有關可滲出物及可浸出物(leachables and extractables)之相關資料,應於何章節段落呈現?
Q38
有關相容性研究之資料,例如凍晶注射劑,於使用前須加入稀釋液配製成注射液,或進一步再調配為輸注液等,探討產品與稀釋液混合之相容性以及安定性等之試驗資料,應於何章節段落呈現?
Q39
3.2.P.3.3製程及製程管制之描述部分,一般化學藥品需要陳述哪些內容?
Q40
如何準備學名藥查驗登記之對照標準品或對照物質資料?