聯絡我們
CONTACT
本平台目的為推廣台灣臨床試驗,提供廠商、研究者及一般民眾臨床試驗之相關訊息。 若您需要刊登受試者招募廣告、臨床試驗相關活動或臨床試驗受托機構訊息,歡迎留下您的資料與聯絡方式,我們會儘速跟您連繫。
若有臨床試驗設計規劃上的諮詢需求,歡迎至財團法人醫藥品查驗中心(CDE)網站的諮詢輔導專區,填寫資料後送出,會有專人與您連繫。
Q11
執行生體相等性試驗之對照藥品規定為何?
Q12
何種學名藥得免除生體相等性試驗?
Q13
監視成分學名藥(含監視期間及監視期滿)的BE試驗及臨床試驗的規定為何?
Q14
非監視成分學名藥是否需要執行生體相等性試驗(BE Study)?
Q15
國內需要執行BA/BE試驗藥品品項為何?
Q16
學名藥查驗登記之安定性試驗資料為何?
Q17
何謂通用技術文件(Common Technical Document, CTD) 格式?
Q18
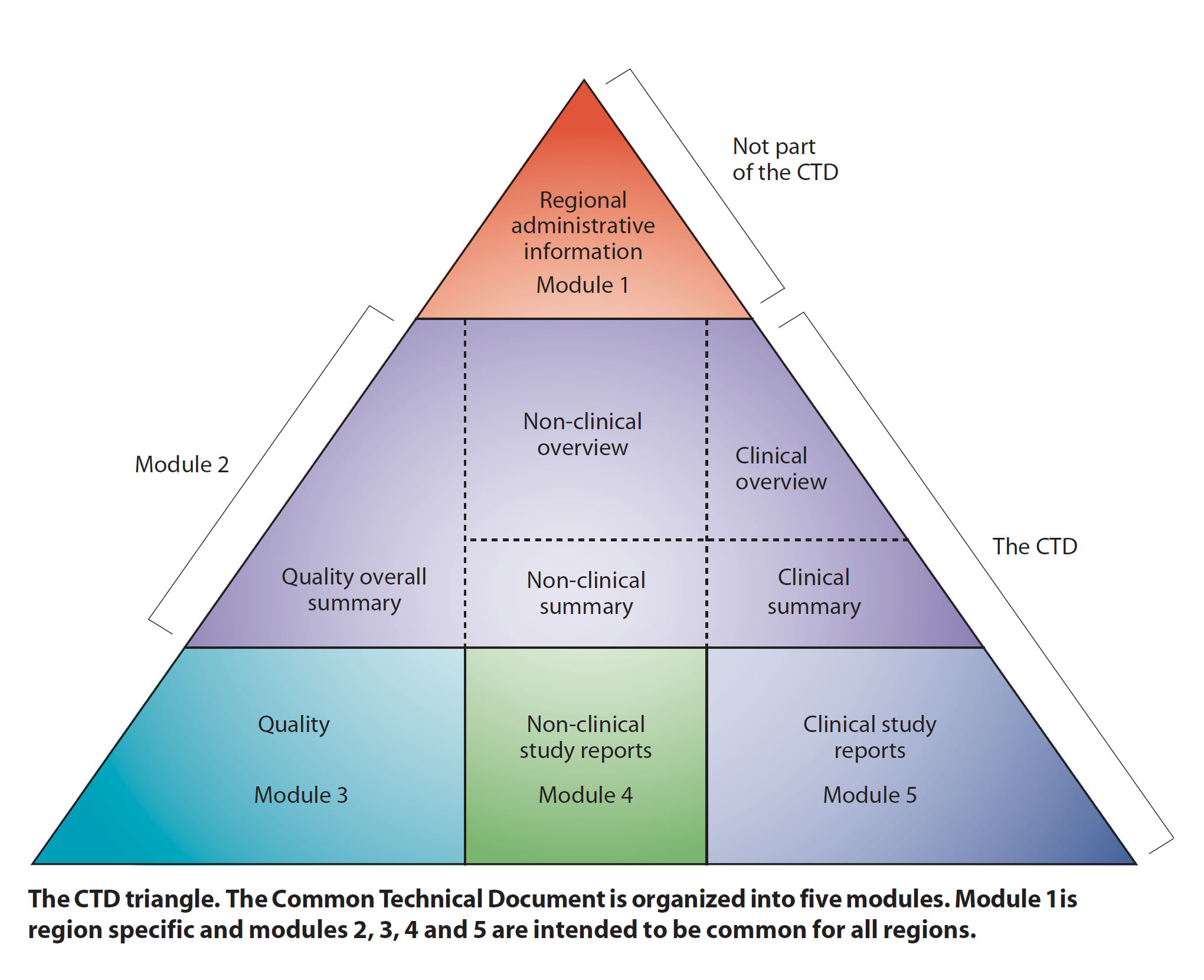
CTD格式的架構為何?
| 模組 | 內容敘述 |
| 模組 1 地區性行政資料(Regional Administrative Information ) | 各地區之行政資料要求 |
| 模組 2 通用技術文件摘要(Summaries) | 藥品品質、非臨床和臨床資料之摘要 |
| 模組 3 品質(Quality) | 藥品原料藥、成品之化學製造管制(CMC)的資料 |
| 模組 4 非臨床試驗報告(Non-Clinical Study Reports) | 在動物體上執行藥理學、毒理學試驗的資料 |
| 模組 5 臨床試驗報告(Clinical Study Reports) | 臨床試驗、人體藥動藥效學試驗的資料 |
Q19
國內學名藥查驗登記採CTD格式送審何時開始實施?
Q20
申請學名藥查驗登記是否可採用e-CTD電子送件方式?